Realizzare uno screening su base nazionale della popolazione di pazienti a rischio di evoluzione verso l’Alzheimer, al fine di ottimizzare la futura distribuzione dei nuovi farmaci che potrebbero arrivare per prevenire o curare la malattia. Ma anche con lo scopo di evitare di esporre al trattamento e alle potenziali correlate reazioni avverse pazienti che non ne trarrebbero giovamento, garantendo così la sostenibilità del sistema.
A questo punta il progetto Interceptor pensato da Aifa e da esperti sulle demenze illustrato oggi al ministero della Salute. Un progetto avviato quindi per essere pronti a gestire l’evenienza dell’arrivo sul mercato di uno o più farmaci per demenza di Alzheimer: nei prossimi anni, infatti, termineranno le sperimentazioni di oltre 50 farmaci potenzialmente in grado di rallentare/arrestare l’Alzheimer.
Ma molti di essi agiranno solo nelle forme “prodromiche” di malattia che appartengono ad una condizione definita Mild Cognitive Impairment (MCI): fondamentale quindi non farsi trovare impreparati e individuare prima i possibili candidati. Per questo il progetto,finanziato con 3,9 milioni di euro, coinvolgerà 400 pazienti con lievi deficit cognitivi, sui quali saranno valutati 7 biomarcatori, per capire appunto quali sono in grado di selezionare con maggiore precisione l’evoluzione della malattia a 3 anni dalla diagnosi.
“L’Alzheimer è la malattia principale in una popolazione anziana come la nostra – ha detto il ministro della Salute, Beatrice Lorenzin – siamo in attesa dei risultati di molte sperimentazioni, che ci fanno sperare che fra il 2018 e il 2025 vedranno la luce prodotti che potranno agire sulla malattia. Hanno però effetti collaterali e aspetti che dobbiamo riuscire a inserire in un processo organizzativo generale, e bisogna partire per tempo. Siamo fra i primi a farlo. Prepariamo il terreno in modo che l’Italia sarà pronta a curare centinaia di migliaia di persone in modo appropriato e sicuro. Quello che vogliamo è cominciare a realizzare nuovi modelli organizzativi che ci permettano di intercettare il malato e i fabbisogni reali il prima possibile, per poter poi agire su questi soggetti a rischio in maniera appropriata. Stiamo iniziando a ragionare in termini di costi evitati e su una nuova governance: non vogliamo lavorare sull’emergenza ma fare una programmazione nel lungo periodo per garantire l’accesso immediato ai farmaci innovativi che arriveranno. Ecco perché occorre intercettare i fabbisogni reali e l’innovatività reale. Così il costo è più sostenibile e ‘spalmabile’ nel tempo”.
“Vogliamo essere i primi e non farci trovare impreparati” ha sottolineato il direttore generale dell’Aifa, Mario Melazzini. “I nuovi farmaci andranno somministrati a chi sta sviluppando la malattia per avere il massimo effetto possibile – ha aggiunto – il nostro compito è quindi fare programmazione e identificare biomarcatori che definiranno questa tipologia di pazienti. Dobbiamo fornire risposte a 600 mila persone e alle loro famiglie e quanto investiamo sarà recuperato in termini di costi indiretti. È una sfida che dobbiamo vincere”.
La Malattia di Alzheimer rappresenta la più frequente patologia neurodegenerativa. La prevalenza della malattia aumenta con l’età e raggiunge il 15-20% nei soggetti di oltre 80 anni. Il problema è destinato a crescere: secondo le stime ogni anno vengono diagnosticati 7,7 milioni di nuovi casi (come dire che ogni 3 secondi viene diagnosticato un nuovo caso) e la sopravvivenza media dopo la diagnosi è oramai di oltre 10 anni.
Oggi purtroppo non esistono farmaci in grado di fermare o far regredire la malattia e tutti i trattamenti disponibili puntano a contenerne i sintomi o limitarne l’aggravarsi per alcuni mesi.
Negli ultimi anni l’approccio più frequente della ricerca è quello di sviluppare un intervento farmacologico precocissimo sulle prime fasi della malattia in cui i sintomi sono minimi. A tal fine, è stata posta maggiore attenzione all’individuazione di biomarcatori che permettano di predire la conversione verso la demenza di Alzheimer dei pazienti con lieve compromissione delle funzioni cognitive (Mild cognitive impairment), ovvero individui con rischio maggiore di sviluppare malattia di Alzheimer (circa 735mila persone in Italia).
Lo studio Interceptor. “Questa è una malattia che lavora nel buio anche 20-25 anni prima della comparsa dei primi sintomi – ha spiegato Paolo Maria Rossini, responsabile Struttura complessa di Neurologia del Policlinico Gemelli di Roma – un lungo periodo che si chiama fase prodromica in cui sintomi sono minimi ma c’è già una malattia che sta lavorando. Attraverso i biomarcatori possiamo indentificare le persone che hanno un elevato rischio di diventare vere e propri dementi. Oggi abbiamo un insieme di dati che ci dicono che ci sono tanti biomarcatori che affiancati a test che già effettuiamo possono dirci quali sono le persone che hanno un elevato rischio di diventare vere e propri dementi. Tutto questo nell’ottica dell’arrivo di nuovi farmaci”.
Nello studio saranno valutati 7 marcatori (selezionati sulla base dell’evidenza scientifica ad oggi disponibile), al fine di stabilire quali siano più sensibili e specifici per predire la conversione del lieve declino cognitivo in demenza di Alzheimer. Nel disegno si tiene conto della fattibilità del progetto e della sostenibilità dei costi. Il costo totale stimato per i 400 pazienti è pari a euro 3.950.000. Il vantaggio in termini sanitari ed economici è evidente se si considera che, in Italia, il numero totale dei pazienti con demenza di Alzheimer (circa la metà di tutte le varie forme di demenza) è stimato in oltre 600mila casi e circa 3 milioni sono le persone direttamente o indirettamente coinvolte nell’assistenza dei loro cari. Stime di calcolo circa i costi socio-sanitari della demenza di Alzheimer ipotizzano cifre complessive pari a circa 6 miliardi.
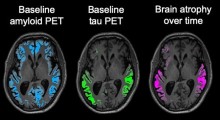
Tutti i pazienti saranno valutati mediante i 7 biomarcatori: alcuni test neuropsicologici, il dosaggio di alcune proteine su campioni di liquor cefalorachidiano, la tomografia ad emissione di positroni (PET), l’analisi genetica, la valutazione del tracciato elettroencefalografico (EEG) per connettività e la risonanza magnetica volumetrica.Inoltre, alcuni campioni biologici (DNA, siero, plasma e liquor) saranno conservati in un biorepository (a -80 °C), pronti per eventuali altri test, se nel prossimo futuro dovessero emergere nuovi marcatori.
I pazienti saranno monitorati per 3 anni, al termine dei quali sarà possibile concludere quale biomarcatore o quale combinazione di biomarcatori, è stato in grado di selezionare con maggior precisione l’evoluzione della malattia a 3 anni dalla diagnosi.
Fonte: Quotidiano Sanità (> English text) - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali colelgamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.









 Associazione Alzheimer OdV
Associazione Alzheimer OdV