Una ricerca appena pubblicata ha rivelato un collegamento stretto tra le proteine associate al morbo di Alzheimer (MA) e la perdita di vista legata all'età. I risultati potrebbero aprire la strada a nuovi trattamenti per i pazienti con deterioramento della vista e attraverso questo studio, gli scienziati ritengono di poter ridurre la necessità di usare animali nelle ricerche future sulla malattie dell'occhio.
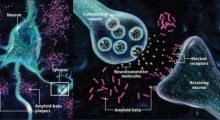
La proteina amiloide-beta (Aβ) è la causa principale del MA, ma comincia anche a raccogliersi nella retina mentre le persone invecchiano. Occhi donati da pazienti che soffrivano di degenerazione maculare legata all'età (DMLE), la causa più comune di cecità degli anziani, hanno dimostrato di avere molta Aβ nella retina.
Questo nuovo studio, pubblicato su Cells, si basa su ricerche precedenti che avevano mostrato che l'Aβ si raccoglie attorno a uno strato di cellule chiamato 'epitelio pigmentato retinico' (EPR), stabilendo quali danni causano alle cellule EPR queste proteine tossiche.
Il team di ricerca ha esposto all'Aβ le cellule EPR di occhi normali di topo e in coltura. Il topo modello ha permesso al team di osservare l'effetto della proteina sul tessuto di occhi viventi, attraverso tecniche di scansione non invasive usate nelle cliniche di oftalmologia. I risultati hanno mostrato che gli occhi del topo sviluppano una patologia retinica sorprendentemente simile alla DMLE degli umani.
La dott.ssa Arjuna Ratnayaka, docente di scienze della vista all'Università di Southampton, che ha guidato lo studio, ha detto:
"Questo è uno studio importante che ha mostrato anche che il numero di topi usati per esperimenti di questo tipo può essere ridotto significativamente in futuro. Siamo riusciti a sviluppare un modello robusto per studiare la patologia retinica simile all'DMLE guidata dall'Aβ senza usare animali transgenici, spesso impiegati dai ricercatori del settore.
"Può servire fino a un anno, e di solito di più, prima che ai topi transgenici, o progettati geneticamente, l'Aβ provochi la patologia nella retina; ora possiamo ottenerlo in 2 settimane. Questo riduce la necessità di sviluppare altri modelli transgenici e migliora il benessere degli animali".
I ricercatori hanno anche usato modelli di cellule, che hanno ulteriormente ridotto l'uso di topi in questi esperimenti, dimostrando che le proteine Aβ tossiche entrano nelle cellule EPR e si raccolgono rapidamente nei lisosomi, il sistema di smaltimento dei rifiuti delle cellule. Anche se le cellule facevano il loro solito lavoro di aumentare gli enzimi all'interno dei lisosomi per scomporre questo carico indesiderato, lo studio ha rilevato che circa l'85% dell'Aβ rimaneva ancora all'interno dei lisosomi, e quindi le molecole tossiche continueranno ad accumularsi nel tempo all'interno delle cellule EPR.
Inoltre, i ricercatori hanno scoperto che una volta che i lisosomi erano invasi dall'Aβ, era disponibile circa il 20% in meno di lisosomi per scomporre i segmenti esterni del fotorecettore, una funzione che eseguono regolarmente nel ciclo visivo giornaliero. La dott.ssa Ratnayaka ha aggiunto:
"Questa è un'ulteriore indicazione del modo in cui le cellule degli occhi possono deteriorarsi nel tempo a causa di queste molecole tossiche che si raccolgono all'interno delle cellule EPR. Questo potrebbe essere un nuovo percorso che nessuno ha esplorato finora.
"Le nostre scoperte hanno anche rafforzato il legame tra le malattie dell'occhio e il cervello. L'occhio fa parte del cervello e abbiamo mostrato che l'Aβ, nota per guidare importanti condizioni neurologiche come il MA, può anche causare danni significativi alle cellule della retina".
I ricercatori sperano che uno dei prossimi passi sia la riproposizione di farmaci anti-Aβ, già sperimentati nei pazienti di MA, e la loro sperimentazione come possibile trattamento per la degenerazione maculare correlata all'età. Poiché i regolatori di farmaci USA e della UE hanno già dato l'approvazione per molti di questi farmaci, questa è un'area che potrebbe essere esplorata con relativa rapidità.
Lo studio può anche aiutare gli sforzi più ampi per superare in gran parte la sperimentazione animale ove possibile, e quindi alcuni aspetti dei test su nuovi trattamenti clinici possono passare direttamente dai modelli cellulari ai pazienti.
Fonte: University of Southampton (> English) - Traduzione di Franco Pellizzari.
Riferimenti: Savannah Lynn, David Johnston, Jenny Scott, Rosie Munday, Roshni Desai, Eloise Keeling, Ruaridh Weaterton, Alexander Simpson, Dillon Davis, Thomas Freeman, David Chatelet, Anton Page, Angela Cree, Helena Lee, Tracey Newman, Andrew Lotery, Arjuna Ratnayaka. Oligomeric Aβ1-42 Induces an AMD-Like Phenotype and Accumulates in Lysosomes to Impair RPE Function. Cells, 2021, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.








 Associazione Alzheimer OdV
Associazione Alzheimer OdV