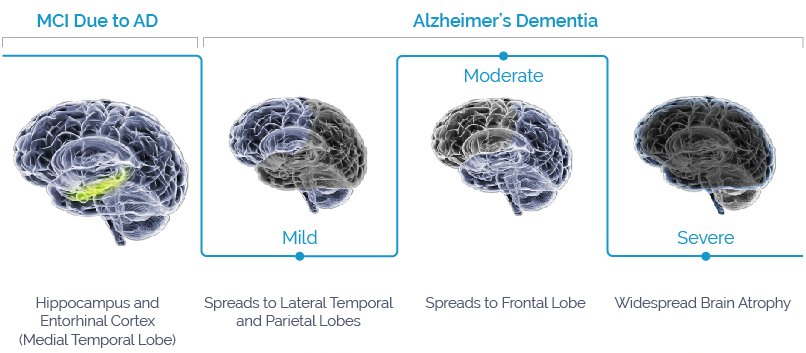
Una collaborazione guidata dalla Cornell University ha usato l'apprendimento automatico per individuare i mezzi e le tempistiche più accurate, per anticipare il progresso del morbo di Alzheimer (MA) nelle persone che sono cognitivamente normali o che hanno un lieve deterioramento cognitivo (MCI, mild cognitive impairment).
La modellazione ha mostrato che prevedere il futuro declino della demenza per gli individui con MCI è più facile e accurato di quanto non sia per gli individui cognitivamente normali o asintomatici. Allo stesso tempo, i ricercatori hanno scoperto che le previsioni per i soggetti cognitivamente normali sono meno accurate per gli orizzonti temporali più lunghi, ma per gli individui con MCI è vero il contrario.
La modellazione ha anche dimostrato che le scansioni a risonanza magnetica (MRI) sono uno strumento prognostico utile per le persone in entrambe le fasi, mentre gli strumenti che tracciano i biomarcatori molecolari, come la tomografia a emissione di positroni (PET), sono più utili per le persone con MCI.
Lo studio del team è pubblicato dal 16 novembre in PLoS One, con primo autore Batuhan Karaman, dottorando di ingegneria elettrica e informatica. Il MA può richiedere anni, a volte decenni, per progredire prima che una persona mostri sintomi. Una volta diagnosticati, alcuni individui declinano rapidamente ma altri possono vivere per anni con sintomi lievi, il che rende difficile prevedere il tasso di avanzamento della malattia.
L'autore senior Mert Sabuncu, professore associato di ingegneria elettrica e informatica della Cornell e di ingegneria elettrica in radiologia alla Weill Cornell Medicine, ha dichiarato:
“Quando possiamo dire con sicurezza che qualcuno ha la demenza, è troppo tardi. Ci sono già molti danni nel cervello, e sono danni irreversibili. Dobbiamo davvero riuscire a cogliere il MA all'inizio, ed essere in grado di dire chi progredirà velocemente e chi più lentamente, in modo da poter stratificare i diversi gruppi di rischio e implementare qualsiasi opzione terapeutica disponibile".
I medici si concentrano spesso su un singolo 'orizzonte temporale', di solito 3/5 anni, per prevedere la progressione del MA in un paziente. Il periodo di tempo può sembrare arbitrario, secondo Sabuncu, il cui laboratorio è specializzato nell'analisi dei dati biomedici, in particolare i dati di scansione, con un'enfasi sulla neuroscienza e la neurologia.
Sabuncu e Karaman hanno collaborato con Elizabeth Mormino dell'Università di Stanford per usare l'apprendimento automatico della rete neurale in grado di analizzare dati di 5 anni su individui cognitivamente normali o con MCI. I dati, tratti da uno studio dell'Alzheimer’s Disease Neuroimaging Initiative, comprendevano tutto, dalla storia genetica di un individuo alle scansioni PET e MRI.
"Quello a cui eravamo veramente interessati è, possiamo guardare questi dati e dire se una persona progredirà nei prossimi anni?", ha detto Sabuncu. "E soprattutto, possiamo fare un lavoro migliore di previsione quando combiniamo tutti i punti di analisi che abbiamo su singoli soggetti?"
I ricercatori hanno scoperto diversi schemi notevoli. Ad esempio, predire che una persona passerà dall'essere asintomatica a mostrare sintomi lievi è molto più facile per un orizzonte temporale di un anno, rispetto a 5 anni. Tuttavia, prevedere se qualcuno declinerà dal MCI alla demenza di MA è più accurato su una sequenza temporale più lunga, con il 'punto critico' a circa 4 anni.
"Questo potrebbe dirci qualcosa sul meccanismo sottostante delle malattie e come si evolve in termini temporali, ma è qualcosa che non abbiamo ancora sondato", ha detto Sabuncu.
Per quanto riguarda l'efficacia dei diversi tipi di dati, la modellazione ha mostrato che le scansioni MRI danno più informazioni per i casi asintomatici e sono particolarmente utili per prevedere se qualcuno svilupperà i sintomi nei prossimi 3 anni, ma meno utili per le previsioni di una persona con MCI. Una volta che un paziente ha sviluppato MCI, le scansioni PET, che misurano alcuni marcatori molecolari come le proteine amiloide e tau, sembrano essere più efficaci.
Un vantaggio dell'approccio dell'apprendimento automatico è che le reti neurali sono abbastanza flessibili da poter funzionare nonostante i dati mancanti, come per i pazienti che potrebbero aver saltato una risonanza magnetica o una PET.
Nel lavoro futuro, Sabuncu prevede di modificare ulteriormente la modellazione in modo che possa elaborare i dati di scansione o genomici completi, piuttosto che solo misurazioni di riepilogo, per raccogliere più informazioni e aumentare l'accuratezza predittiva.
Fonte: David Nutt in Cornell University (> English) - Traduzione di Franco Pellizzari.
Riferimenti: BK Karaman, EC Mormino, MR Sabuncu. Machine learning based multi-modal prediction of future decline toward Alzheimer’s disease: An empirical study. PLOS ONE, 2022, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.






 Associazione Alzheimer OdV
Associazione Alzheimer OdV