 Ricercatori del Medical Center della Columbia University (CUMC) hanno identificato un difetto nelle proteine di traffico all'interno delle cellule cerebrali, che può essere alla base di forme comuni non-familiari del Parkinson.
Ricercatori del Medical Center della Columbia University (CUMC) hanno identificato un difetto nelle proteine di traffico all'interno delle cellule cerebrali, che può essere alla base di forme comuni non-familiari del Parkinson.
Il difetto è sul punto di convergenza dell'azione di almeno tre differenti geni che erano stati implicati nella malattia da studi precedenti. Mentre la maggior parte degli studi molecolari si sono concentrati sulle mutazioni associate a rare forme familiari della malattia, questi risultati si riferiscono direttamente alla forma comune non-familiare di Parkinson.
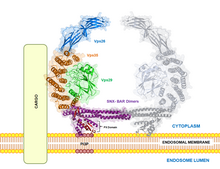
Lo studio è stato pubblicato ieri, 6 Febbraio, nell'edizione online della rivista Neuron. Il percorso difettoso è chiamato percorso "retromer", in parte perché può guidare il riutilizzo di molecole chiave spostandole indietro dalla superficie cellulare ai depositi interni. In questo studio, i difetti nella via retromer sembrano avere profondi effetti sul macchinario cellulare di eliminazione dei rifiuti, fatto che può spiegare perché le cellule cerebrali nel Parkinson, in ultima analisi, accumulano grandi aggregati di proteine. I difetti di traffico associati al Parkinson possono essere invertiti aumentando l'attività del percorso retromer, suggerendo una possibile strategia terapeutica. Nessuna delle attuali terapie per il Parkinson altera la progressione della malattia.
I ricercatori hanno anche trovato la prova che queste modifiche molecolari sono al lavoro anche negli individui sani che portano semplicemente varianti genetiche comuni associate ad un maggiore rischio di Parkinson, suffragando la tesi che approcci terapeutici precoci saranno importanti nella lotta contro la malattia. "Nel loro insieme, i risultati suggeriscono che farmaci che colpiscano il percorso retromer potrebbero aiutare a prevenire o curare il Parkinson", scrive il responsabile dello studio Asa Abeliovich, MD, PhD, professore associato di patologia e biologia cellulare e di neurologia al Taub Institute for Research on Alzheimer's Disease and Aging Brain del CUMC.
Negli ultimi anni, attraverso studi sul genoma (GWAS), i ricercatori hanno identificato circa 10 varianti genetiche comuni che sembrano avere piccoli effetti sul rischio di Parkinson non-familiare, e tuttavia è stato difficile approfondire l'impatto di queste varianti. "Esaminando il tessuto cerebrale del paziente durante l'autopsia, di solito è troppo tardi, tutti i neuroni critici della dopamina se ne sono andati da molto tempo e il danno è stato fatto", ha detto il Dott. Abeliovich.
In questo studio, il dottor Abeliovich e i suoi colleghi del CUMC, hanno utilizzato una serie insolitamente ampia di approcci: comprese le analisi di varianti genetiche associate al Parkinson, tessuto cerebrale dei pazienti, studi in vitro sul tessuto di coltura di neuroni cerebrali, e modelli di moscerino della frutta (Drosophila) che ospitano varianti genetiche collegate a quelle associata al Parkinson.
I ricercatori hanno scoperto che delle varianti comuni in due geni precedentemente legati al Parkinson (LRRK2 e RAB7L1) hanno avuto un impatto inaspettatamente simile nel tessuto cerebrale umano. Gli effetti delle varianti sono altamente coincidenti, indicando un percorso di azione comune. Sono stati osservati importanti cambiamenti cellulari nel percorso retromer, che è coinvolto nel traffico di proteine dall'apparato Golgi (che impacchetta le proteine da consegnare agli altri elementi cellulari) ai lisosomi (che riciclano proteine ed altre molecole).
Sono stati trovate anche mutazioni che influenzano il percorso retromer nel Parkinson familiare. Studi precedenti del Taub Institute della Columbia hanno dimostrato che le varianti genetiche dei geni associati con la funzione retromer sono collegati all'Alzheimer e i livelli del componente retromer appaiono alterati nel cervello di Alzheimer, suggerendo un ruolo più ampio della disfunzione del retromer nelle malattie neurodegenerative dell'invecchiamento, secondo il dottor Abeliovich.
L'impatto delle varianti RAB7L1 e LRRK2 è evidente anche negli individui senza segni o sintomi di Parkinson. Ciò suggerisce l'esistenza di un pre-stato di malattia nei portatori sani delle due varianti genetiche, che favorisce l'insorgenza precoce della malattia e che, in teoria, potrebbe essere mirato terapeuticamente. I ricercatori del CUMC hanno anche dimostrato che la sovraespressione di una delle due varianti (la RAB7L1) può superare gli effetti dell'altra variante. Analogamente, l'espressione del VPS35, un gene coinvolto nel percorso retromer, può sopprimere patologia dell'LRRK2 mutante. "Sarà interessante sviluppare farmaci che puntano direttamente a questi componenti retromer o che, più in generale, promuovono il flusso attraverso la via", scrive il Dott. Abeliovich.
Gli altri partecipanti allo studio sono David A. Macleod, Herve Rhinn, Tomoki Kuwahara, Ari Zolin, Gilbert Di Paolo, Brian D. McCabe, Lorrain N. Clark, e Scott A. Small, tutti del CUMC. Lo studio è stato finanziato dalla Fondazione Michael J. Fox e dal National Institutes of Health.
***********************
Cosa pensi di questo articolo? Ti è stato utile? Hai rilievi, riserve, integrazioni? Conosci casi o ti è successo qualcosa che lo conferma? o lo smentisce? Puoi usare il modulo dei commenti qui sotto per dire la tua opinione. Che è importante e unica.
***********************
Fonte: Materiale del Columbia University Medical Center.
Riferimento: David A. MacLeod, Herve Rhinn, Tomoki Kuwahara, Ari Zolin, Gilbert Di Paolo, Brian D. MacCabe, Karen S. Marder, Lawrence S. Honig, Lorraine N. Clark, Scott A. Small, Asa Abeliovich. RAB7L1 Interacts with LRRK2 to Modify Intraneuronal Protein Sorting and Parkinson's Disease Risk. Neuron, 2013; 77 (3): 425 DOI: 10.1016/j.neuron.2012.11.033.
Pubblicato in Science Daily il 6 Febbraio 2013 - Traduzione di Franco Pellizzari - Foto: Complesso retromer da Wikipedia
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari proposti da Google sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.
| Sostieni l'Associazione; una donazione, anche minima, ci aiuterà ad assistere malati e famiglie e continuare ad informarti. Clicca qui a destra: |



 Associazione Alzheimer OdV
Associazione Alzheimer OdV