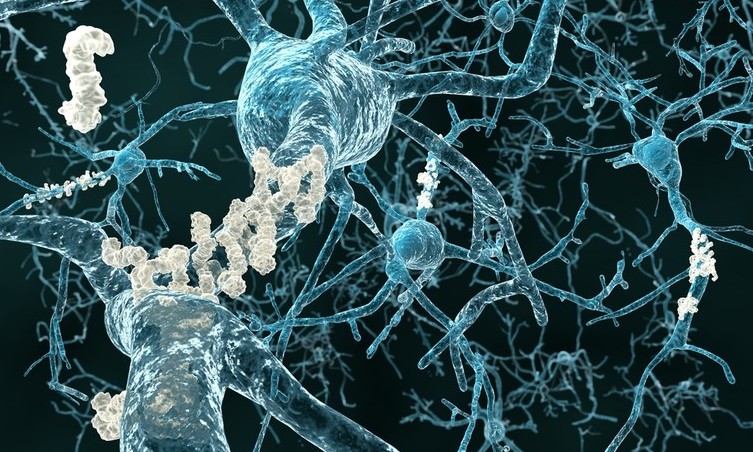
 Neuroni con placche di amiloide-beta (Fonte: Juan Gaertner/Shutterstock.com)
Neuroni con placche di amiloide-beta (Fonte: Juan Gaertner/Shutterstock.com)
Anche se le cause dell'Alzheimer rimangono un mistero, la ricerca genetica sta ora fornendo indizi su come si sviluppa la malattia. Sappiamo che delle mutazioni genetiche rare possono causare l'Alzheimer ad esordio precoce, ma nella forma più comune ad insorgenza tardiva sono coinvolti sia fattori genetici che ambientali.
Raccogliendo informazioni sul patrimonio genetico di migliaia di persone, gli scienziati nel nostro gruppo e di altri, hanno identificato quasi 30 varianti del gene che sono più comuni nella malattia. La funzione nel cervello di molti di questi "geni di rischio" non è nota, ma sembrano raggrupparsi per funzione biologica, dandoci una maggiore comprensione dei meccanismi coinvolti nell'Alzheimer.
Una delle funzioni biologiche implicate da queste scoperte genetiche nella malattia è il trasporto di materiale nella cellula, noto come endocitosi. Questo avviene quando il materiale non può attraversare passivamente la membrana cellulare e la cellula si protrae verso l'interno per catturare il carico in un piccolo sacco pieno di liquido.
Il nostro gruppo di ricerca sta studiando cosa fanno questi geni endocitici nel cervello. Con l'uso di cellule coltivate in un piatto, possiamo manipolare le proteine che essi esprimono e misurare le variazioni nell'assorbimento di materiale da parte della cellula. Questo ci aiuta a capire che cosa accade quando questi geni sono alterati nell'Alzheimer.
L'endocitosi è una funzione delle cellule universalmente importante: tutte le cellule hanno bisogno di mangiare e bere. E' anche responsabile di molti altri compiti vitali, compresa la comunicazione, il trasporto e l'eliminazione di prodotti di scarto, come l'amiloide-beta. Questa è una proteina prodotta nel cervello sano che viene di norma scomposta ed eliminata. Nell'Alzheimer, tuttavia, si ritiene che uno squilibrio della produzione di amiloide-beta, e nella sua rimozione dal cervello, provochi il suo accumulo, con la formazione di grumi appiccicosi (placche), che sono tossici per i neuroni.
Lavori di pulizia del cervello
Rastrellare l'amiloide-beta è una delle funzioni delle microglia, le cellule immunitarie del cervello che reagiscono per prime quando un intruso entra nel cervello. Usano le loro capacità endocitiche per inghiottire e distruggere il materiale di scarto e gli agenti infettivi. Nell'Alzheimer, questa funzione è fondamentale, visto che consumano l'amiloide-beta, scomponendola attraverso il loro sistema interno di smaltimento dei rifiuti.
L'amiloide-beta può essere rimossa anche attraverso i 650 km di vasi sanguigni di tutto il cervello umano. Le cellule endoteliali che rivestono i vasi formano una barriera ermetica tra il sangue e il cervello. Questa ferma gli agenti tossici, ma permette alle sostanze nutritive di entrare e ai prodotti di scarto di uscire.
L'amiloide-beta viene rimossa dal cervello con una forma speciale di endocitosi che coinvolge il suo legame ad un recettore sulla superficie delle cellule endoteliali, come una serratura con la sua chiave. Questo innesca la sua internalizzazione ed è trasportata attraverso la cellula e depositata nel sangue, impedendone l'accumulo nel cervello.
Come arriva lì l'amiloide-beta all'inizio?
La funzione precisa dell'amiloide-beta non è ancora chiara, ma è probabile che abbia un ruolo nella normale fisiologia del cervello, e che diventi un problema solo quando è presente in eccesso. È prodotta dalla scissione della «proteina precursore dell'amiloide» (APP), presente sulla superficie delle cellule del cervello.
L'APP può essere scissa in due modi diversi, uno solo dei quali produce amiloide-beta. L'enzima responsabile di questo percorso risiede all'interno della cellula, quindi l'APP deve subire l'endocitosi per essere rotta in frammenti di amiloide-beta.
Parte della nostra ricerca riguarda la misurazione della quantità di amiloide-beta e di altri frammenti prodotti dalle cellule in seguito alla scissione dell'APP. Confrontandoli tra le cellule sane e quelle in cui i geni di rischio di Alzheimer sono stati manipolati, potremo capire il coinvolgimento di questi geni nella produzione di amiloide-beta. Qui, ancora una volta, l'endocitosi appare un giocatore fondamentale per il potenziale sviluppo di Alzheimer.
Quanto sopra descrive solo tre esempi dell'importanza dell'endocitosi per la salute del cervello e come un guasto in uno di questi meccanismi potrebbe essere un fattore che contribuisce allo sviluppo di Alzheimer. In realtà gli studi genetici hanno implicato molti altri processi biologici ed è improbabile che questi siano mutuamente esclusivi.
Se aggiungiamo i fattori dello stile di vita e di rischio ambientale, l'Alzheimer è molto complesso. Tuttavia, attraverso la comprensione dei vari meccanismi coinvolti, possiamo cominciare a identificare dei bersagli potenziali per il trattamento. Proprio come facciamo in un puzzle, stiamo usando le informazioni genetiche come pezzi angolari per costruire un quadro più chiaro della malattia nel suo complesso.
Fonte: Anna Burt PhD, ricercatrice della Cardiff University
Pubblicato in The Conversation (> English text) - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.




 Associazione Alzheimer OdV
Associazione Alzheimer OdV