Uno studio eseguito alla Università della California di San Diego ha identificato il PKCα come un potenziale bersaglio terapeutico nell'Alzheimer.
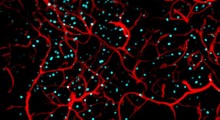
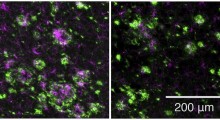
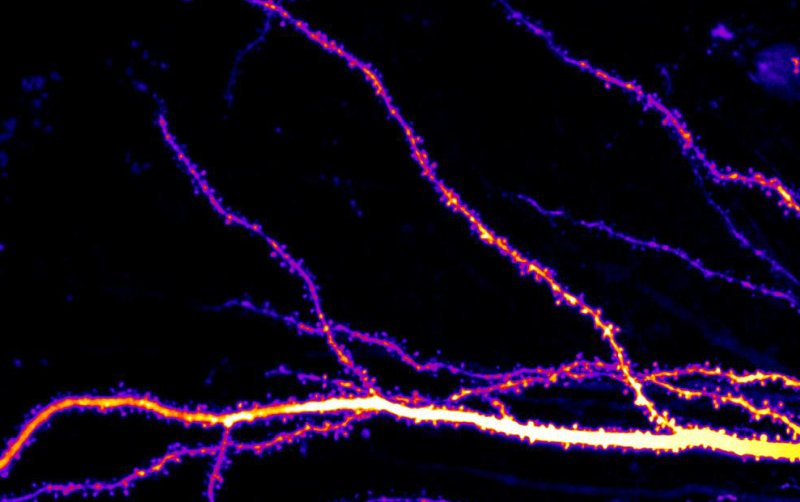 I neuroni dell'ippocampo nei topi PKCA M489V mostrano meno spine dendritiche rispetto ai topi di controllo di tipo selvaggio (Fonte: UC San Diego).
I neuroni dell'ippocampo nei topi PKCA M489V mostrano meno spine dendritiche rispetto ai topi di controllo di tipo selvaggio (Fonte: UC San Diego).
In una ricerca recente di varianti geniche associate al morbo di Alzheimer (MA), diverse famiglie colpite hanno mostrato una mutazione in un enzima chiamato 'proteina chinasi C-alfa' (PKCα): i membri della famiglia con questa mutazione avevano il MA, mentre quelli senza la mutazione non avevano la malattia.
La mutazione M489V ha da tempo dimostrato di aumentare l'attività del PKCα di un modesto 30%, ma era finora poco chiaro se e come contribuisce alla neuropatologia del MA. In un nuovo studio, ricercatori dell'Università della California di San Diego hanno scoperto che il tenue aumento del PKCα era sufficiente per produrre deterioramenti biochimici, cellulari e cognitivi nei topi, simili a quelli osservati nel MA umano.
I risultati dello studio, pubblicati il 23 novembre 2022 su Nature Communications, posizionano il PKCα come un promettente bersaglio terapeutico per la malattia. Il PKCα regola la funzione di molte altre proteine, in particolare nel cervello. L'enzima facilita le reazioni chimiche che aggiungono gruppi di fosfato ad altre proteine, modellando la loro attività e la capacità di legarsi ad altre molecole.
Regolando lo stato di fosforilazione delle proteine nell'ambiente sinaptico, il PKCα può avere un ruolo importante nella funzione sinaptica e nella segnalazione neuronale. Per valutare tale ruolo nel MA, diversi team di ricerca hanno collaborato per generare prima un topo modello con la mutazione PKCα M489V e quindi per valutare la sua biochimica e il suo comportamento nel corso dell'anno e mezzo successivo (corrispondente a circa 55 anni nell'invecchiamento umano).
Dopo tre mesi, il cervello dei topi mutati presentava livelli significativamente alterati di fosforilazione delle proteine rispetto al cervello dei topi di controllo di tipo selvaggio, indicando che le proteine neuronali venivano regolate erroneamente. A 4,5 mesi, i neuroni ippocampali dei topi hanno mostrato diversi cambiamenti cellulari, tra cui depressione sinaptica e ridotta densità delle spine dendritiche. A 12 mesi, i topi hanno mostrato prestazioni compromesse nei test comportamentali di apprendimento spaziale e di memoria, prove chiare del declino cognitivo.
"Siamo rimasti sorpresi di scoprire che è stato sufficiente solo un leggero aumento dell'attività di PKCα per ricreare il fenotipo del MA in un topo", ha dichiarato l'autrice senior Alexandra C. Newton PhD, prof.ssa illustre di farmacologia della UC San Diego. "Questo è un esempio straordinario dell'importanza dell'omeostasi in biologia: anche piccoli modifiche nell'attività delle chinasi possono provocare una patologia, se si permette agli effetti di accumularsi nel corso della vita".
Per confermare se simili cambiamenti enzimatici erano presenti nei pazienti umani, i ricercatori hanno misurato i livelli di proteina nella corteccia frontale del cervello umano di pazienti deceduti con MA e di individui di controllo. I cervelli di pazienti con MA hanno mostrato un aumento del 20% di PKCα. In più, la fosforilazione di un substrato PKCα noto era aumentata di circa quattro volte in questi cervelli, suggerendo così che l'attività di PKCα è enfatizzata nel cervello di MA umano.
"La mutazione PKCα M489V è stata un ottimo modo per testare il ruolo di questo enzima nel MA, ma ci sono molti altri modi per avere PKCα aberrante", ha affermato la Newton. "Stiamo scoprendo che molte mutazioni associate al MA si trovano in geni che regolano il PKCα, quindi varie varianti geniche potrebbero effettivamente convergere su questo stesso percorso importante".
Gli autori notano che diversi farmaci inibitori del PKCα sono già stati sviluppati per il cancro e potrebbero essere riproposti per il trattamento del MA. Lo sviluppo futuro di farmaci potrebbe concentrarsi su modi per inibire selettivamente il PKCα nelle sinapsi.
"È sempre più chiaro che le placche amiloidi che vediamo nel MA sono secondarie ad altri processi precedenti nel cervello", ha affermato la Newton. "I nostri risultati si aggiungono a un corpo crescente di prove che il PKCα può essere una parte importante di quel processo ed è un obiettivo promettente per il trattamento o la prevenzione del MA".
Fonte: Nicole Mlynaryk in University of California - San Diego (> English) - Traduzione di Franco Pellizzari.
Riferimenti: G Lordén, ...[+7], RE Tanzi, AC Newton. Enhanced activity of Alzheimer disease-associated variant of protein kinase Cα drives cognitive decline in a mouse model. Nature Comm., 2022, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.








 Associazione Alzheimer OdV
Associazione Alzheimer OdV