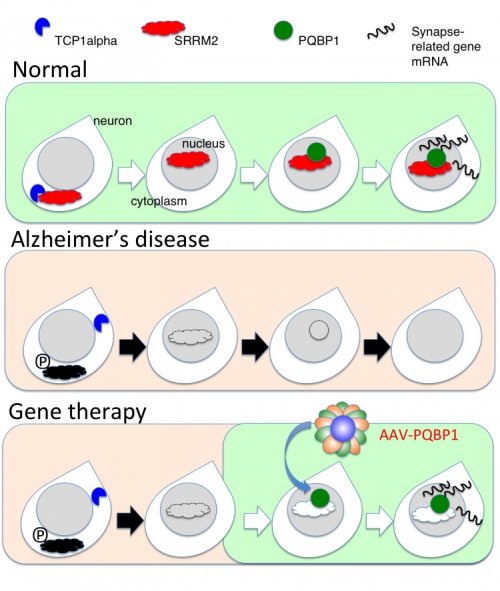
 Teoria della terapia genica AAV-PQBP1: nell'Alzheimer sono deficitari sia la proteina SRRM2 della scaffalatura del nucleo, sia il regolatore genetico delle sinapsi PQBP1. Aumentando la proteina PQBP1 nei neuroni, si recupera l'espressione genetica delle sinapsi e si invertono i difetti cognitivi nei pazienti di Alzheimer.Il morbo di Alzheimer (MA) è la forma più comune di demenza, che coinvolge la perdita di memoria e una riduzione delle capacità cognitive.
Teoria della terapia genica AAV-PQBP1: nell'Alzheimer sono deficitari sia la proteina SRRM2 della scaffalatura del nucleo, sia il regolatore genetico delle sinapsi PQBP1. Aumentando la proteina PQBP1 nei neuroni, si recupera l'espressione genetica delle sinapsi e si invertono i difetti cognitivi nei pazienti di Alzheimer.Il morbo di Alzheimer (MA) è la forma più comune di demenza, che coinvolge la perdita di memoria e una riduzione delle capacità cognitive.
I pazienti con MA sviluppano molteplici strutture proteiche anormali nel loro cervello che si pensa possano distruggere o danneggiare le cellule nervose (neuroni).
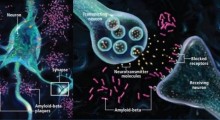
Una di queste strutture, la placca senile, è costituita da gruppi di peptide amiloide-beta (Aβ) che si formano negli spazi tra i neuroni.
Molti studi clinici avanzati in pazienti con MA hanno tentato di rallentare o invertire la malattia puntando tali placche per rimuoverle. Tuttavia, nonostante il successo nel diminuire l'aggregazione dell'Aβ, questi studi hanno per lo più fallito nel migliorare la memoria o la funzione cognitiva nei pazienti con MA.
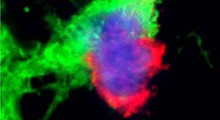
Prima che avvenga la formazione degli aggregati di Aβ, gli studi hanno rivelato cambiamenti nella fosforilazione (una modifica chimica) di alcune proteine, tra cui la SRRM2. Si pensava che questa proteina fosse coinvolta in una forma di regolazione genica chiamata splicing, ma la sua funzione esatta non era chiara.
Ora, un team giapponese di ricercatori guidati dalla Tokyo Medical and Dental University ha esaminato i livelli di fosforilazione della SRRM2 in un topo modello di MA e ha scoperto che sono aumentati già prima dell'aggregazione dell'Aβ. Questo alla fine impedisce il trasporto nel nucleo della SRRM2 e porta a livelli ridotti di proteina PQBP1, che è stata collegata con disturbi intellettuali e del neurosviluppo. I risultati dello studio sono riferiti in Molecular Psychiatry.
"Abbiamo dimostrato che l'aumento di fosforilazione della SRRM2 le impediva di interagire con un'altra proteina che aiuta il ripiegamento delle proteine", dice il primo autore Hikari Tanaka. "In assenza di questa interazione, la SRRM2 rimane non ripiegata, quindi non è trasportata nel nucleo ed è degradata nel citoplasma".
Il team ha poi misurato i livelli delle proteine SRRM2 e PQBP1 nella corteccia cerebrale dei topi con MA di fase iniziale e dei pazienti con MA di stadio terminale umano, nonché nelle cellule iPS umane di MA. Entrambe le proteine erano notevolmente ridotte rispetto alle quantità corrispondenti nei controlli sani.
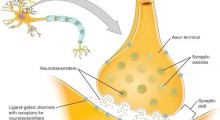
"Per scoprire quale effetto avrebbe avuto una riduzione della PQBP1 in vivo, abbiamo generato topi mancanti del gene PQBP1", spiega l'autore corrispondente Hitoshi Okazawa. "Abbiamo osservato un declino cognitivo e cambiamenti nella morfologia delle loro sinapsi, che sono giunzioni tra neuroni che consentono la comunicazione elettrica e chimica. Questi cambiamenti sono causati da modelli interrotti di splicing del gene delle sinapsi".
Hanno usato un vettore virale contenente PQBP1 per recuperare l'espressione della proteina sinapsi in questi topi. Non solo ha ripristinato l'espressione della PQBP1, ma ha anche recuperato i fenotipi anomali.
Questi risultati offrono una nuova visione dei primi cambiamenti che si verificano durante la patologia di MA che coinvolgono le proteine di splicing, suggerendo possibilità di terapie geniche con vettori di virus.
Fonte: Tokyo Medical and Dental University (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Hikari Tanaka, Kanoh Kondo, Xigui Chen, Hidenori Homma, Kazuhiko Tagawa, Aurelian Kerever, Shigeki Aoki, Takashi Saito, Takaomi Saido, Shin-ichi Muramatsu, Kyota Fujita, Hitoshi Okazawa. The intellectual disability gene PQBP1 rescues Alzheimer’s disease pathology. Molecular Psychiatry, 2018; DOI: 10.1038/s41380-018-0253-8
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.







 Associazione Alzheimer OdV
Associazione Alzheimer OdV