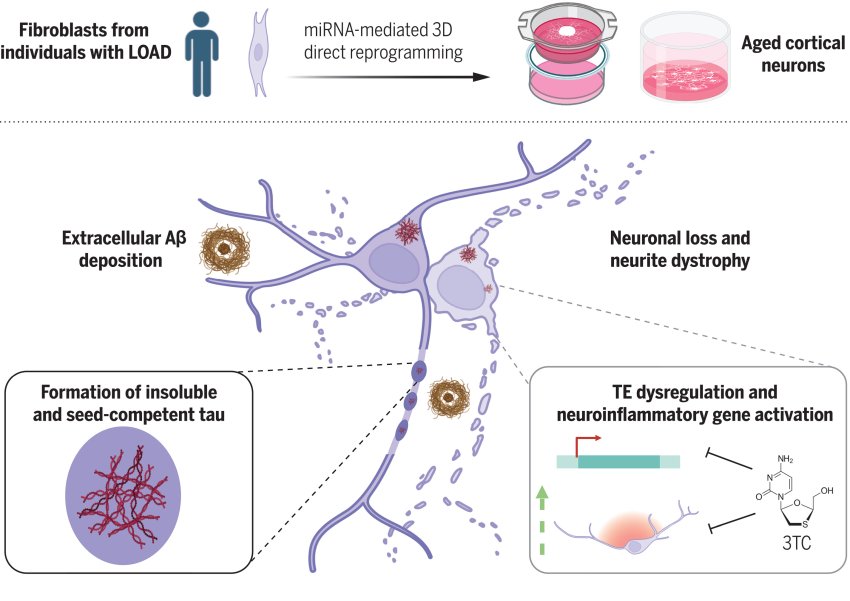
 Schema grafico dello studio Zhao Sun et al
Schema grafico dello studio Zhao Sun et al
Ricercatori della Washington University di St. Louis hanno sviluppato un modo per cogliere gli effetti dell'invecchiamento nello sviluppo del morbo di Alzheimer (MA): hanno ideato un metodo per studiare i neuroni anziani in laboratorio senza biopsia cerebrale, un progresso che potrebbe contribuire a una migliore comprensione della malattia e a nuove strategie di trattamento.
Gli scienziati hanno trasformato le cellule della pelle prelevate da pazienti con MA ad esordio tardivo in cellule cerebrali chiamate neuroni. Il MA ad esordio tardivo si sviluppa gradualmente per molti decenni e inizia a mostrare sintomi solo dopo i 65 anni. Per la prima volta, questi neuroni derivati in laboratorio hanno accuratamente riprodotto i segni distintivi di questo tipo di demenza, che includono l'accumulo di amiloide-beta (Aβ), depositi di proteine tau e morte delle cellule neuronali.
Studiando queste cellule, i ricercatori hanno identificato aspetti dei genomi delle cellule, chiamati elementi retrotrasposibili (che cambiano la loro attività con l'età), nello sviluppo del MA ad esordio tardivo. I risultati, pubblicati su Science, suggeriscono nuove strategie di trattamento che puntano questi fattori.
"Il MA sporadico e ad esordio tardivo è il tipo più comune della malattia, rappresentando oltre il 95% dei casi", ha affermato l'autore senior Andrew Yoo PhD, professore di biologia dello sviluppo. “È stato finora molto difficile da studiare in laboratorio a causa della complessità della malattia, che deriva da vari fattori di rischio, incluso l'invecchiamento. Fino ad ora, non avevamo il modo di cogliere gli effetti dell'invecchiamento nelle cellule per studiare il MA ad esordio tardivo".
Gli studi fatti fino ad oggi su animali modello di MA si sono concentrati, per necessità, sui topi con mutazioni genetiche rare, note per causare il MA ereditato e ad esordio precoce in persone giovani, una strategia che ha fatto luce sulla condizione ma differisce dal suo sviluppo nella gran parte dei pazienti con la forma sporadica ad esordio tardivo. Per riprodurre più fedelmente possibile la malattia in laboratorio, il team di Yoo si è rivolto a un approccio chiamato 'riprogrammazione cellulare'.
Il metodo per trasformare direttamente in neuroni le cellule ottenute facilmente dalla pelle umana di pazienti in vita, consente di studiare gli effetti del MA sul cervello senza i rischi della biopsia cerebrale e conservando le conseguenze dell'età del paziente sui neuroni. Il lavoro passato di Yoo e dei suoi colleghi, che ha aperto la strada a questa tecnica di trasformazione usando piccole molecole di RNA chiamate microRNA, si era concentrato sulla comprensione dello sviluppo della malattia di Huntington, una condizione neurologica ereditaria che in genere mostra sintomi di insorgenza nell'età adulta.
Dopo aver trasformato le cellule della pelle in cellule cerebrali, i ricercatori hanno scoperto che i nuovi neuroni possono crescere in uno strato di gel sottile o auto-assemblarsi in piccoli gruppi -chiamati sferoidi - imitando l'ambiente 3D del cervello. I ricercatori hanno confrontato gli sferoidi neuronali generati da pazienti con MA sporadico ad esordio tardivo, con MA ereditato e da coetanei sani.
Gli sferoidi dei pazienti con MA hanno rapidamente sviluppato depositi di Aβ e grovigli tau tra i neuroni. È emersa anche l'attivazione di geni associati all'infiammazione, quindi i neuroni hanno iniziato a morire, imitando ciò che si vede nelle scansioni cerebrali dei pazienti. Gli sferoidi dei donatori più vecchi e sani nello studio hanno mostrato una deposizione di Aβ ma molto minore di quella dei pazienti. I piccoli depositi di Aβ negli sferoidi più vecchi e sani sono la prova che la tecnica sta cogliendo gli effetti dell'età e suggeriscono che l'accumulo di Aβ e tau era correlato all'invecchiamento. Dimostra inoltre che il processo di MA peggiora molto l'accumulo anomalo.
I ricercatori, che includono il primo autore Zhao Sun PhD, del laboratorio di Yoo, hanno scoperto che il trattamento degli sferoidi dei pazienti con MA ad esordio tardivo, con farmaci che interferiscono con la formazione dell'Aβ all'inizio del processo della malattia, prima che i neuroni inizino ad accumulare Aβ tossica, ha ridotto significativamente i depositi di Aβ. Ma il trattamento in tempi successivi, dopo che era già presente un po' di accumulo, non ha avuto alcun effetto o ha ridotto solo modestamente i depositi conseguenti di Aβ. Tali dati sottolineano l'importanza di identificare e curare presto la malattia.
Lo studio ha inoltre trovato un ruolo degli elementi retrotrasposibili, piccoli pezzi di DNA che saltano in diversi punti del genoma, nello sviluppo del MA ad esordio tardivo. L'inibizione di tali 'geni che saltano' con il farmaco lamivudina (o 3TC) un anti-retrovirale che può smorzare l'attività degli elementi retrotrasposibili, ha avuto un effetto positivo: gli sferoidi dei pazienti con MA ad esordio tardivo hanno ridotto l'Aβ e i grovigli di tau e hanno provocato meno morte neuronale rispetto agli stessi sferoidi trattati con un placebo.
Il trattamento con lamivudina non ha avuto alcun effetto benefico sugli sferoidi ottenuti da pazienti con MA ereditato ad esordio precoce, fornendo prove del fatto che lo sviluppo del MA ad esordio tardivo sporadico, correlato all'invecchiamento, ha caratteristiche molecolari distinte dal MA autosomico ereditario.
"In questi pazienti, il nostro nuovo sistema modello ha identificato un ruolo degli elementi retrotrasposibili associati al processo della malattia", ha affermato Yoo. “Siamo stati lieti di vedere che potremmo ridurre il danno con un trattamento farmacologico che sopprime questi elementi. Non vediamo l'ora di usare questo sistema modello per nuovi interventi terapeutici personalizzati del MA ad esordio tardivo".
I ricercatori stanno pianificando studi futuri con sferoidi che includono più tipi di cellule cerebrali, inclusi neuroni e glia.
Fonte: Washington University in St. Louis via Neuroscience News (> English) - Traduzione di Franco Pellizzari.
Riferimenti: Z Sun, [+18], AS Yoo. Modeling late-onset Alzheimer’s disease neuropathology via direct neuronal reprogramming. Science, 2024, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.














 Associazione Alzheimer OdV
Associazione Alzheimer OdV