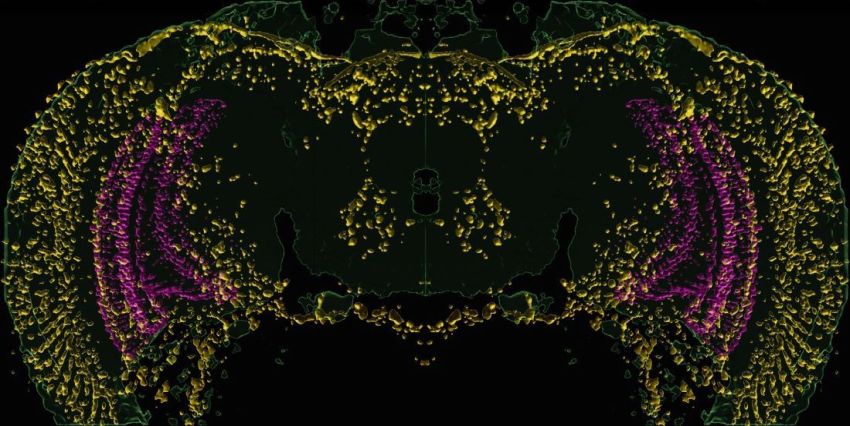
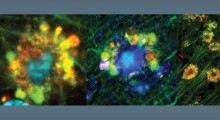
 In giallo proteine correlate allo stress che si accumulano nel cervello di un moscerino della frutta con vista deteriorata.
In giallo proteine correlate allo stress che si accumulano nel cervello di un moscerino della frutta con vista deteriorata.
Ricercatori del centro medico della University of Texas Southwestern di Dallas (Texas/USA) hanno collegato la cecità in animali modello a una risposta allo stress cellulare nel cervello che è un fattore di rischio comune della demenza. I loro risultati, pubblicati su Nature Communications, potrebbero aiutare a spiegare la connessione tra perdita di vista o udito e demenza.
"Il nostro studio fornisce informazioni meccanicistiche su come la compromissione sensoriale può essere un potenziale fattore di rischio per la demenza e sottolinea anche l'importanza di ripristinare o mantenere i sistemi sensoriali per ridurre al minimo le complicanze", ha affermato Helmut Krämer PhD, professore di neuroscienze e biologia cellulare della UT Southwestern, che ha guidato lo studio con Katherine Wert PhD, assistente prof.ssa di oftalmologia e biologia molecolare, e con il post-dottorato Shashank Shekhar PhD.
Nell'ultimo decennio, i ricercatori hanno scoperto che le persone con perdita di vista o udito hanno più probabilità di sviluppare la demenza. Studi hanno stimato che la perdita di udito in mezza età contribuisce all'8,2% dei casi di demenza in tutto il mondo e che la compromissione della vista è associata all'1,8% dei casi di demenza in USA. Tuttavia, il meccanismo biologico alla base di questo legame era ancora sconosciuto.
Studiando la segnalazione molecolare nei moscerini della frutta, i dott. Krämer e Shekhar e i loro colleghi hanno fatto una scoperta casuale: il cervello dei moscerini della frutta geneticamente modificati per essere ciechi avevano una diffusa 'risposta integrata allo stress' (ISR).
La ISR protegge le cellule di tutto il corpo da condizioni come fame, infezione virale e deprivazione di ossigeno, limitando la produzione di proteine delle cellule e accendendo geni che riparano il danno cellulare, ha spiegato il dott. Krämer. Se la ISR rimane attiva per periodi prolungati, può uccidere le cellule attraverso l'apoptosi, un meccanismo che elimina le cellule danneggiate impossibilitate a riprendersi, e che minacciano le cellule vicine. Di conseguenza, la ISR è associata a disturbi neurodegenerativi, che includono l'Alzheimer e altre forme di demenza.
Sebbene i ricercatori abbiano visto proteine che propagano la ISR, chiamate ATF4 e XRP1, in tutto il cervello dei moscerini ciechi, erano in un punto improbabile. Piuttosto che essere nel nucleo delle cellule colpite, dove in genere influenzano i geni coinvolti nella ISR, ATF4 e XRP1 sono state trovate in condensati molecolari. Queste goccioline all'interno di una cellula rimangono separate dagli altri contenuti, proprio come l'olio nell'acqua.
Quando i ricercatori nel laboratorio della Wert hanno esaminato il cervello dei topi portatori di mutazioni genetiche che avevano indotto la cecità, hanno visto un fenomeno simile. I condensati avevano una stretta somiglianza con i granuli di stress, una gocciolina simile che si forma all'interno delle cellule nervose sotto stress. Quando i ricercatori hanno usato un farmaco noto per dissolvere questi granuli di stress, si sono sciolti anche i condensati che legavano ATF4 e XRP1, suggerendo che condensati e granuli di stress potrebbero condividere lo stesso scopo.
Non è ancora chiaro come tali condensati possano stimolare la demenza se si sviluppano nel cervello dei pazienti con cecità o altre menomazioni sensoriali, ha affermato il dott. Krämer. Un'ipotesi è che inibire l'entrata nel nucleo cellulare alle proteine che propagano la ISR potrebbe inizialmente essere protettivo, evitando la ISR a lungo termine, e la conseguente apoptosi. Tuttavia, i condensati potrebbero impedire alle proteine associate alla ISR di rispondere ad altre complicanze neurali, come la sovrapproduzione di proteine associate all'Alzheimer, rendendo le cellule più vulnerabili ai danni.
Studi futuri valuteranno se dissolvere i condensati molecolari potrebbe avere un effetto positivo o negativo sulla neurodegenerazione, ha affermato la dott.ssa Wert.
Fonte: UT Southwestern Medical Center (> English) - Traduzione di Franco Pellizzari.
Riferimenti: S Shekhar, [+4], H Krämer. Sensory quiescence induces a cell-non-autonomous integrated stress response curbed by condensate formation of the ATF4 and XRP1 effectors. Nat Commun, 2025, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.





 Associazione Alzheimer OdV
Associazione Alzheimer OdV