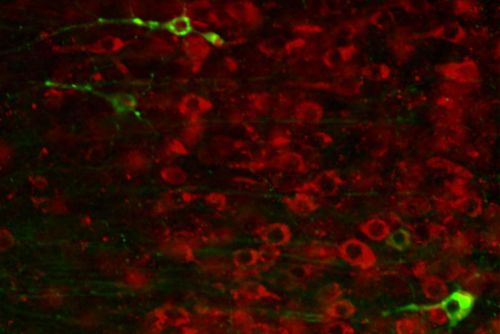
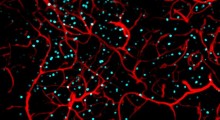
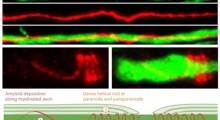
 Nei neuroni che contengono il farmaco (sopra, in rosso) non ci sono grovigli di tau (in verde).In circostanze normali, la proteina tau contribuisce al funzionamento normale e sano dei neuroni del cervello.
Nei neuroni che contengono il farmaco (sopra, in rosso) non ci sono grovigli di tau (in verde).In circostanze normali, la proteina tau contribuisce al funzionamento normale e sano dei neuroni del cervello.
In alcune persone, però, si raccoglie in grovigli tossici che danneggiano le cellule cerebrali. Tali grovigli sono una caratteristica dell'Alzheimer e di altre malattie neurodegenerative.
Ma i ricercatori della Washington University di St. Louis hanno dimostrato che i livelli della proteina tau possono essere ridotti - e alcuni dei danni neurologici causati da tau addirittura invertiti - da una molecola sintetica che punta le istruzioni genetiche della formazione della tau, prima della sua produzione.
Lo studio, eseguito nei topi e nelle scimmie, è stato pubblicato il 25 gennaio su Science Translational Medicine. I risultati suggeriscono che la molecola, chiamata «oligonucleotide antisenso», potrebbe in potenza trattare le malattie neurodegenerative caratterizzate da tau anomala, compreso l'Alzheimer.
"Abbiamo dimostrato che questa molecola abbassa i livelli della proteina tau, prevenendo e, in alcuni casi, invertendo il danno neurologico", ha detto Timothy Miller MD/PhD, professore di neurologia e autore senior dello studio. "Questo composto è il primo a dimostrare di invertire i danni legati alla tau nel cervello, con il potenziale per essere usato come terapeutico nelle persone".
Miller, con Sarah DeVos PhD e i colleghi, hanno studiato dei topi modificati geneticamente che producono una forma mutante di tau umana che si raggruma facilmente insieme. Questi topi iniziano a mostrare i grovigli di tau intorno ai 6 mesi di età e esibiscono un po' di danno neuronale dai 9 mesi.
Per ridurre la tau, i ricercatori hanno usato un oligonucleotide antisenso, una sorta di molecola che interferisce con le istruzioni della costruire delle proteine. I geni nel DNA vengono copiati nel RNA, una molecola messaggero che porta le istruzioni per costruire una proteina. Gli oligonucleotidi antisenso si legano all'RNA messaggero e lo distruggono prima che la proteina possa essere formata. Tali oligonucleotidi possono essere progettati per puntare l'RNA per quasi tutte le proteine.
I ricercatori hanno somministrato ogni giorno, per un mese, una dose di oligonucleotide anti-tau a topi di 9 mesi e hanno poi misurato la quantità di RNA tau, di proteine totali tau e di grovigli di proteine tau nel cervello quando i topi avevano 12 mesi di età. Tutti e tre i livelli si sono ridotti significativamente nei topi trattati, rispetto ai topi che hanno ricevuto un placebo.
È importante sottolineare che i livelli di tau totale e di grovigli tau nel cervello dei topi di 12 mesi trattati erano inferiori a quelli di 9 mesi non trattati, il che suggerisce che il trattamento non solo aveva fermato, ma aveva invertito l'accumulo di tau.
Nel momento in cui questo ceppo di topi geneticamente modificati raggiunge i 9 mesi di età, l'ippocampo (una parte del cervello importante per la memoria) di solito è visibilmente rimpicciolito e evidenzia neuroni morenti. Ma con il trattamento via oligonucleotide, sono stati bloccati sia il restringimento che la morte cellulare. Non c'era, però, alcuna prova di inversione della morte neuronale.
I topi trattati hanno vissuto in media 36 giorni in più rispetto ai topi non trattati, ed erano più bravi a costruire nidi, fatto che riflette una combinazione di comportamento sociale, prestazioni cognitive e capacità motorie. Tutte queste funzioni possono essere compromesse nelle persone con Alzheimer e con altre malattie neurodegenerative correlate alla tau.
I trattamenti con oligonucleotide di recente sono stati approvati dalla Food and Drug Administration per due malattie neuromuscolari: distrofia muscolare di Duchenne e atrofia muscolare spinale (SMA). L'oligonucleotide per la SMA è stato scoperto dalla Ionis Pharmaceuticals, che ha collaborato con Miller per sviluppare il trattamento oligonucleotide per le malattie neurologiche da tau. La Washington University detiene brevetti congiunti con la Ionis Pharmaceuticals per l'uso di oligonucleotidi per ridurre i livelli di tau.
Sono in corso esperimenti umani di oligonucleotidi per diverse altre malattie neurologiche, tra cui il morbo di Huntington e la sclerosi laterale amiotrofica (SLA) o morbo di Lou Gehrig. Miller è uno degli autori dell'esperimento della SLA.
Miller e colleghi si sono incuriositi della possibilità di progettare studi per abbassare la tau nelle persone, ma prima avevano bisogno di vedere come funziona l'oligonucleotide in un animale più simile alle persone di un topo.
I ricercatori hanno trattato gruppi di scimmie di tipo 'macaco cinomolgo' (Macaca fascicularis) con due dosi di placebo o oligonucleotide, a una settimana di distanza, direttamente nel liquido cerebrospinale che circonda il midollo spinale e il cervello, proprio come si dovrebbe fare con i pazienti umani. Due settimane più tardi, hanno misurato la quantità di proteine tau e di RNA nel cervello delle scimmie e nel liquido cerebrospinale.
L'oligonucleotide ha ridotto sia l'RNA che le proteine tau nel cervello, e tale riduzione si è riflessa nel fluido cerebrospinale. "Lo studio sulle scimmie ci ha dimostrato che meno tau nel liquido cerebrospinale si correla a meno tau nel cervello", ha detto Miller. "Questo è importante se vogliamo valutare questo approccio terapeutico nelle persone, perché non c'è un modo non invasivo per misurare i livelli di tau nel cervello. Questa correlazione ci dice che possiamo usare i livelli della proteina tau nel liquido cerebrospinale come misura dei livelli di tau nel cervello".
I grovigli di tau sono associati non solo all'Alzheimer, ma a una serie di malattie neurodegenerative meno note, come la paralisi sopranucleare progressiva e degenerazione corticobasale. I livelli di tau aumentano anche a seguito di lesioni cerebrali traumatiche, che possono portare alla demenza.
"I grovigli di tau si correlano con il declino cognitivo in diverse malattie", ha detto Miller. "Questo è un nuovo approccio promettente per ridurre la tau, ma dobbiamo verificare se è sicuro nelle persone, e se abbassa realmente la tau, come è stato progettato per fare, prima di arrivare alla domanda se ha un qualsiasi effetto sulla malattia. Ma tutto quello che abbiamo visto finora dice che questo vale la pena di essere indagato come potenziale trattamento per le persone".
Fonte: Tamara Bhandari in Washington University (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Sarah L. DeVos, Rebecca L. Miller, Kathleen M. Schoch, Brandon B. Holmes, Carey S. Kebodeaux, Amy J. Wegener, Guo Chen, Tao Shen, Hien Tran, Brandon Nichols, Tom A. Zanardi, Holly B. Kordasiewicz, Eric E. Swayze, C. Frank Bennett, Marc I. Diamond, Timothy M. Miller. Tau reduction prevents neuronal loss and reverses pathological tau deposition and seeding in mice with tauopathy. Science Translational Medicine, 2017; 9 (374): eaag0481 DOI: 10.1126/scitranslmed.aag0481
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.




 Associazione Alzheimer OdV
Associazione Alzheimer OdV