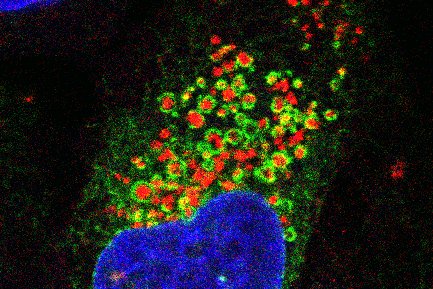
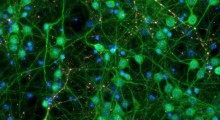
 La microscopia a fluorescenza mostra la rete del reticolo endoplasmatico (verde) che si avvolge attorno ai lisosomi danneggiati (rosso). Il nucleo cellulare è in blu (Fonte: Jay Xiaojun Tan)
La microscopia a fluorescenza mostra la rete del reticolo endoplasmatico (verde) che si avvolge attorno ai lisosomi danneggiati (rosso). Il nucleo cellulare è in blu (Fonte: Jay Xiaojun Tan)
Ricercatori dell'Università di Pittsburgh hanno descritto per la prima volta sulla rivista Nature un percorso attraverso il quale le cellule riparano i danni ai lisosomi, le strutture che, riciclando la spazzatura cellulare, contribuiscono alla longevità. I risultati sono un passo importante verso la comprensione e il trattamento delle malattie legate all'età guidate dai lisosomi con fuoriuscite.
"Il danno ai lisosomi è un segno distintivo dell'invecchiamento e di molte malattie, in particolare dei disturbi neurodegenerativi come il morbo di Alzheimer (MA)", ha dichiarato il primo autore Jay Xiaojun Tan PhD, assistente professore di biologia cellulare e membro dell'Aging Institute, una partnership tra la Pitt e il suo centro medico. "Il nostro studio identifica una serie di passaggi che crediamo costituiscano un meccanismo universale per la riparazione lisosomiale, che abbiamo chiamato percorso PITT, per ricordare l'Università di Pittsburgh".
Come sistema di riciclaggio della cellula, i lisosomi contengono potenti enzimi digestivi che degradano i rifiuti molecolari. A questi contenuti viene impedito di danneggiare altre parti della cellula, con una membrana che agisce da recinzione attorno a una struttura per rifiuti pericolosi. Sebbene in questa recinzione possano verificarsi rotture, una cellula sana ripara rapidamente il danno. Per saperne di più su questo processo di riparazione, Tan ha collaborato con l'autore senior Toren Finkel MD/PhD, direttore dell'Aging Institute e professore illustre di medicina alla Pitt.
Innanzitutto, Tan ha danneggiato sperimentalmente i lisosomi in cellule coltivate in laboratorio e poi ha misurato le proteine che sono arrivate sulla scena. Ha scoperto che un enzima chiamato PI4K2A si è accumulato in pochi minuti sui lisosomi danneggiati e ha generato livelli alti di una molecola di segnalazione chiamata PtdIns4P.
“La PtdIns4P è come una spia rossa che dice alla cellula "Ehi, abbiamo un problema qui", ha detto Tan. "Questo sistema di allerta recluta quindi un altro gruppo di proteine chiamate ORP".
Le proteine ORP funzionano come catene, ha spiegato Tan. Un'estremità della proteina si lega alla spia rossa PtdIns4P sul lisosoma e l'altra estremità si lega al reticolo endoplasmatico, la struttura cellulare coinvolta nella sintesi di proteine e lipidi.
"Il reticolo endoplasmatico è avvolto attorno al lisosoma come una coperta", ha aggiunto Finkel. "Normalmente, il reticolo endoplasmatico e i lisosomi si toccano a malapena, ma una volta che il lisosoma è stato danneggiato, abbiamo scoperto che si stavano abbracciando".
Attraverso questo abbraccio, il colesterolo e un lipide chiamato fosfatidilserina sono spinti verso il lisosoma e aiutano a rattoppare i fori nella recinzione della membrana. La fosfatidilserina attiva anche una proteina chiamata ATG2, che agisce da ponte per trasferire altri lipidi nel lisosoma, la fase finale di riparazione della membrana nel percorso PITT (phosphoinositide-initiated membrane tethering and lipid transport) appena descritto.
"La cosa bella di questo sistema è che tutti i componenti del percorso PITT erano già noti, ma non si sapeva che interagivano in questa sequenza, né la loro funzione nella riparazione del lisosoma", ha affermato Finkel. "Credo che questi risultati avranno molte implicazioni per l'invecchiamento normale e per le malattie legate all'età".
I ricercatori sospettano che nelle persone sane, piccole rotture nella membrana del lisosoma siano rapidamente riparate attraverso il percorso PITT. Ma se il danno è troppo esteso o il percorso di riparazione è compromesso - a causa dell'età o di una malattia - i lisosomi che perdono si accumulano. Nel MA, la perdita di fibrille tau dai lisosomi danneggiati è un passo chiave nella progressione della malattia.
Quando Tan ha eliminato il gene che codifica il primo enzima nel percorso, PI4K2A, ha scoperto che la diffusione della fibrilla tau aumentava drasticamente, suggerendo che i difetti nel percorso PITT potrebbero contribuire alla progressione del MA. Nel lavoro futuro, i ricercatori prevedono di sviluppare modelli di topo per capire se il percorso PITT può proteggere i topi dal MA.
Fonte: University of Pittsburgh (> English) - Traduzione di Franco Pellizzari.
Riferimenti: J Xiaojun Tan & T Finkel. A phosphoinositide signalling pathway mediates rapid lysosomal repair. Nature, 7 Sep 2022, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.







 Associazione Alzheimer OdV
Associazione Alzheimer OdV