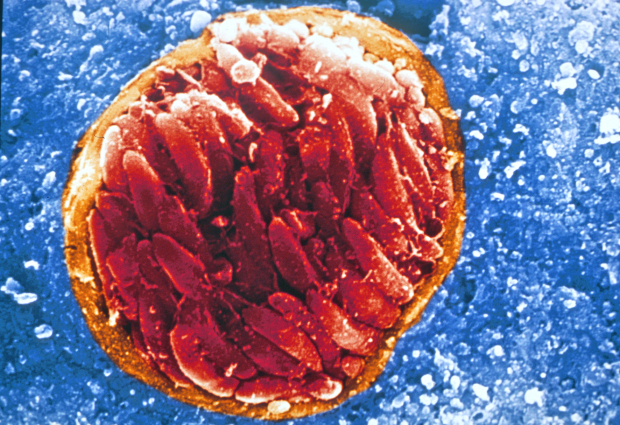
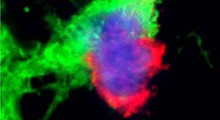
 Il protozoo Toxoplasma gondii, cisti tissutale nel cervello (Foto: D. Ferguson, Oxford University)
Il protozoo Toxoplasma gondii, cisti tissutale nel cervello (Foto: D. Ferguson, Oxford University)
Più di 2 miliardi di persone - quasi un essere umano su tre della terra - hanno un'infezione permanente con il parassita Toxoplasma gondii che dimora nel cervello.
Nel numero di Scientific Reports del 13 settembre 2017, 32 ricercatori di 16 istituzioni diverse descrivono gli sforzi per capire come l'infezione con questo parassita può alterare e in alcuni casi amplificare diversi disturbi cerebrali, tra cui l'epilessia, l'Alzheimer, il Parkinson e alcuni tumori.
Quando una donna è infettata dal T. gondii durante la gravidanza, e passa il parassita al suo bambino non ancora nato, le conseguenze possono essere profonde, inclusi danni devastanti al cervello, al sistema nervoso e agli occhi.
Tuttavia, c'è sempre più evidenza che acquisire questa infezione in vita potrebbe essere lungi dall'essere innocuo. Così i ricercatori hanno cominciato a cercare collegamenti tra questa infezione cronica, ma apparentemente dormiente, e il suo potenziale di alterare il corso di disturbi neurologici comuni.
Rima McLeod MD, professoressa di oftalmologia e scienze visive e pediatria, e direttrice medica del Centro Toxoplasmosi all'Università di Chicago, ha affermato:
"Volevamo capire come questo parassita, che vive nel cervello, possa contribuire a far luce sulla patogenesi di altre malattie cerebrali.
"Sospettiamo che coinvolga più fattori. Al nucleo c'è l'allineamento delle caratteristiche del parassita stesso, dei geni che esprime nel cervello infetto, dei geni di suscettibilità che potrebbero limitare la capacità dell'ospite di prevenire l'infezione e dei geni che controllano la suscettibilità ad altre malattie presenti nell'ospitante umano.
"Altri fattori possono includere la gravidanza, lo stress, le infezioni addizionali e un microbioma insufficiente. Abbiamo ipotizzato che quando questi fattori confluiscono, può insorgere una malattia".
Da più di un decennio i ricercatori notano sottili manipolazioni del comportamento associate a un'infezione latente di T. gondii. Ratti e topi che portano questo parassita, per esempio, perdono l'avversione per l'odore dell'urina di gatto. Questo è pericoloso per un roditore, perché lo rende preda e cibo più facile per i gatti.
Ma dà benefici ai gatti che hanno un pasto, così come ai parassiti, che ottengono un nuovo ospite che li distribuirà ampiamente nell'ambiente. Un gatto infettato acutamente può espellere fino a 500 milioni di oocisti (spore che sopravvivono fuori dell'organismo ospitante) in poche settimane. Anche un solo oocysta, che può rimanere nel suolo o nell'acqua per un anno, è infettivo.
Uno studio più recente ha trovato una connessione simile nei primati. Gli scimpanzé infetti perdono l'avversione al profumo di urina del loro predatore naturale, il leopardo.
Il gruppo di ricerca ha deciso di cercare effetti simili nelle persone. Si sono concentrati su ciò che chiamano 'infettoma' umano, cioè i legami plausibili tra le proteine secrete dal parassita, i microRNA umani espressi, la chimica neurale dell'ospitante umano e i molteplici percorsi che sono perturbati dalle interazioni ospitante-parassiti.
Usando dati raccolti dal National Collaborative Chicago-Based Congenital toxoplasmosis Study, che ha diagnosticato, trattato e seguito 246 persone infette congenitamente e le loro famiglie dal 1981, hanno eseguito un'analisi completa dei sistemi, considerando una gamma di biomarcatori generati da parassiti e valutando il loro impatto probabile.
Lavorando con il J Craig Venter Institute e l'Institute of Systems Biology Scientists, hanno esaminato l'effetto delle infezioni delle cellule staminali neuronali primarie del cervello umano in coltura tissutale, concentrandosi sull'espressione genica e le proteine perturbate. Parte del team, tra cui Huan Ngo della Northwestern University, Hernan Lorenzi del J Craig Venter Institute, Kai Wang e Taek-Kyun Kim dell'Institute for Systems Biology e la McLeod, ha integrato la genetica dell'ospite, la proteomica, la transcrittomica e i dati microRNA circolanti, per costruire un modello di questi effetti sul cervello umano.
Usando un approccio che hanno chiamato di 'ricostruzione e deconvoluzione', i ricercatori hanno identificato i percorsi perturbati associati alle malattie neurodegenerative, nonché i collegamenti tra toxoplasmosi, disturbi del cervello umano e alcuni tumori.
Hanno anche scoperto che:
- Piccoli biomarcatori regolatori (frazioni di microRNA o proteine presenti nei bambini con toxoplasmosi grave) corrispondono a quelli che si trovano in pazienti con malattie neurodegenerative come l'Alzheimer o il Parkinson.
- Il parassita riesce a manipolare 12 recettori olfattivi umani in modi che simulano lo scambio gatto-topo o scimpanzé-leopardo.
- C'è l'evidenza che il gondii potrebbe aumentare il rischio di epilessia, "possibilmente alterando la segnalazione GABAergica".
- L'infezione da gondii è associata a una rete di 1.178 geni umani, molti dei quali sono modificati in diversi tumori.
Scrivono gli autori:
"I nostri risultati forniscono informazioni sui meccanismi con cui, in alcune circostanze, questo parassita potrebbe causare queste malattie associate. Questo lavoro fornisce una mappa dei sistemi per progettare medicinali e vaccini per riparare e prevenire gli effetti neuropatologici del T. gondii sul cervello umano".
Il co-autore Dennis Steinler PhD, direttore del Laboratorio di Neuroscienze e Invecchiamento della Tufts University, ha affermato:
"Questo studio è un cambiamento di paradigma. Ora dobbiamo inserire la malattia infettiva nell'equazione delle malattie neurodegenerative, dell'epilessia e dei tumori neurali".
"Allo stesso tempo, dobbiamo tradurre gli aspetti di questo studio in trattamenti preventivi che includono tutto, dai farmaci alla dieta, allo stile di vita, per ritardare l'insorgenza e la progressione delle malattie".
Fonte: John Easton in University of Chicago (> English text) - Traduzione di Franco Pellizzari.
Reference: Huân M. Ngô, Ying Zhou, Hernan Lorenzi, Kai Wang, Taek-Kyun Kim, Yong Zhou, Kamal El Bissati, Ernest Mui, Laura Fraczek, Seesandra V. Rajagopala, Craig W. Roberts, Fiona L. Henriquez, Alexandre Montpetit, Jenefer M. Blackwell, Sarra E. Jamieson, Kelsey Wheeler, Ian J. Begeman, Carlos Naranjo-Galvis, Ney Alliey-Rodriguez, Roderick G. Davis, Liliana Soroceanu, Charles Cobbs, Dennis A. Steindler, Kenneth Boyer, A. Gwendolyn Noble, Charles N. Swisher, Peter T. Heydemann, Peter Rabiah, Shawn Withers, Patricia Soteropoulos, Leroy Hood, Rima McLeod. Toxoplasma Modulates Signature Pathways of Human Epilepsy, Neurodegeneration & Cancer. Scientific Reports, 2017; 7 (1) DOI: 10.1038/s41598-017-10675-6
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali colelgamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.






 Associazione Alzheimer OdV
Associazione Alzheimer OdV